说明:
1. 翻译自Theusinger OM, Spahn DR.Perioperative blood conservation strategies for major spine surgery.Best Pract Res Clin Anaesthesiol,2016,30(1):41-52.
一、摘要
- 背景:骨科,特别是脊柱和脊柱畸形手术,可能与围术期较多的出血有关。
- 为了降低过量出血和不必要的输血的风险,已经开发了诸如患者血液管理(包括目标导向的凝血管理)策略。
- 最近的研究结果:异体输血的不良反应已经在包括骨科在内的大多数外科领域得到证实。
- 已经做了一些努力来增加术前红细胞(RBC)数量,减少术中出血,并使用限制性输血触发器(restrictive transfusion triggers)以最小化或避免输红细胞。
- 减少术中出血的措施包括:
- 新的手术技术
- 尽可能使用围术期血液回收(use of cell salvage where possible)
- 使用床旁定点设备(point-of-care devices)进行床旁凝血管理
- 凝血因子替代品(substitution of coagulation factors)
- 抗纤维蛋白溶解剂(antifibrinolytic agents)
- 去氨加压素(desmopressin)
- 控制性低血压(induced hypotension)
- 避免体温过低
二、前言
- 随着人们对于同种异体输血(allogeneic blood transfusion)不良后果的认识和证据不断增加,因此要采取措施,尽量减少脊柱大手术过程中的出血。
- 实现这一目标需要全科医生(general practitioners),脊柱外科医生和麻醉医生的共同努力。
- 自2010年以来,世界卫生组织(世卫组织)敦促其成员国使用输血替代品并制定个性化的患者血液管理计划,从而减少输血的需求。
- 患者血液管理的三大支柱是:
- (1)检测和治疗术前贫血
- (2)减少围术期红细胞(RBC)损失
- (3)利用和优化患者特异性贫血的生理储备(包括限制性血红蛋白输血触发器)
- 标准凝血试验(Standard coagulation
tests)被广泛用于鉴别术中凝血功能障碍,但这些试验在出血活跃患者中的价值是值得怀疑的。
- 常规凝血试验(Routine coagulation tests)并非开发用于监测手术室中的出血患者。
- 出于这个原因,下列定点床旁设备越来越多地用于治疗术中出血,并事实上建议用于协助描述凝血障碍和指导止血治疗(hemostatic
therapy)。
- 旋转血栓弹力图(rotational thromboelastometry)
- 血栓弹性描记图(thrombelastography)
- platelet mapping
- 本综述的目的是强调下述内容,以减少出血和输血的需求,从而改善结果:
- 患者血液管理的重要性
- 抗纤溶药物的使用
- 床边定点检测(point-of-care testing)
- 基于算法的凝血因子浓缩物(algorithm-based treatment with factor concentrates)治疗
- 此外,还将讨论在择期脊柱手术的背景下,对使用抗凝血药物患者的管理,对相对较低的血红蛋白水平的耐受程度,局部止血剂和围术期血液回收。
三、检测和治疗术前贫血
在骨科手术中,WHO定义的术前贫血的患病率在文献中报道为20%~50%。
女性为12g/dL,男性为13g/dL
术前贫血是所有手术患者30天内死亡率和发病率增加的独立危险因素。
- 这些患者中有多达三分之一的人贫血是因为缺铁导致的。
- 因此目标是在预定的手术前尽早发现这些患者,以纠正贫血。
- 为了达到最佳效果,治疗应在手术前至少4周开始。
在脊柱手术之前优化红细胞数量作为患者血液管理计划的第一个支柱至关重要,因为这与90天后改善的结果有关。据Theusinger等人最近的一项研究,在瑞士苏黎世的Orthopedic Balgrist大学医院进行的这项程序是可行的。
- 计划进行择期手术(髋,膝和脊柱)的患者由其全科医生筛选血红蛋白(hemoglobin)和铁蛋白水平(ferritin levels)。
- 在贫血的情况下,应推迟手术,并需要进一步评估以确定其原因,例如肿瘤,胃肠道出血等。
- 开始使用静脉注射的铁剂,维生素B12,叶酸和促红细胞生成素治疗,并在2周后检查效果。大多数患者单次治疗就足够了。
- Theusinger等人的结果与Rosencher等人报告得一致。其中一至两剂红细胞生成素足以使血红蛋白增加至非贫血水平。
- 尽管所提到的治疗方法似乎很简单,但它们需要外科医生,麻醉医生和全科医生之间的密切合作。
- 管理一个单位红细胞的大致费用为700-1200美元,相关副作用的治疗可能须另外花费高达1000美元。
- 主要的成本驱动因素(cost drivers)是:
- 复合发病率(composite morbidity)(34%)
- 返回手术室(12.3%)
- 脓毒症(sepsis)(10.5%)
- 肺部问题(15.7%)
- 伤口问题(11.2%)
- 主要的成本驱动因素(cost drivers)是:
与此相比,建议用下列方法治疗的费用约为850美元,因此这显然是有利的方法,因为它仍然比一个单位的红细胞及其副作用便宜:
- 40.000 IU的促红细胞生成素α(erythropoietin alpha)
- 1 g静脉注射铁剂
- 维生素B12(皮下注射)
- 叶酸
四、减少围术期红细胞(RBC)损失
(一)抗纤溶药物(Antifibrinolytic drugs)
- 抗纤溶药物通过抑制血凝块降解(clot degradation)来减少围手术期出血和输血需求。40多年来,这些药物已被用于心脏和大型骨科手术和肝移植,并已被证实有效。
- 所有这些都是赖氨酸样药物(lysine-like drugs),如:
- 抑肽酶(aprotinin)
- 氨甲环酸(tranexamic acid)
- 氨基己酸(aminocaproic acid)
- 这些药物与纤溶酶原的赖氨酸位点(lysine site of plasminogen)结合,从而抑制纤维蛋白溶解酶(ibrinolytic enzyme plasmin)(纤溶酶原+及其激活剂t-PA)使其不能进一步降解纤维蛋白。
- 鉴于Mangano在心脏外科研究中的安全问题,2007年从市场上撤回了抑肽酶(aprotinin)。
- 与其他三组相比,接受抑肽酶组的肾功能衰竭,心肌梗死或心力衰竭(+ 55%)和中风(+ 181%)显着增加。
- 其他三组为:
- 对照组
- 氨甲环酸组(TXA; trans-4-aminomethylcyclohexane-1-carboxylic acid)
- 氨基己酸组(aminocaproic acid)
- 尽管在某些国家重新引入心脏手术,但抑肽酶不再适用于脊柱手术的日常临床实践。
- 然而,在1950年,赖氨酸类似物TXA首先由Okamoto描述,并且在目前广泛应用于创伤,心脏和骨科手术。
- 在脊柱手术中,预防性使用高剂量TXA治疗(1g,然后100mg/h直到缝合)可以显著减少出血和血液(自体血液)输血的需要。术中和术后并发症无显著的差异。
- 同样,Thompson et al.和Dhawale et al.证实了ε-氨基己酸(epsilon
aminocaproic acid,EACA)对脊柱侧凸患者进行脊柱融合的疗效。
- Yuan et al.的meta分析表明抗纤溶剂能够有效减少脊柱手术中的出血量和红细胞输血,与TXA相比,EACA具有更好的效果,但差异不显著。
- 对于脊柱手术的抗纤溶剂用多少剂量比较合适目前尚在争论中,尽管Karski
et al.用增加的剂量实现了更好的疗效。
- 然而,对104项随机试验的系统评价发现,手术出血量的显著减少在很大程度上与静脉注射的TXA的剂量无关(从5.5 mg/kg到300mg/kg)。作者得出结论,对于大多数成年患者,总剂量为1克就足够了。
- Farrokhi等人在他们的研究中使用低剂量TXA(10mg/kg),但在脊柱内固定中的出血和输血要求方面没有观察到显著的效果。
- 问题是大多数研究都是回顾性的,实际上没有关于足够剂量(adequate dose)的明确证据(clear evidence)。
- 目前的证据是,TXA可减少出血,输血量和脊柱手术中的输血率,而不会增加任何并发症。
- 由于TXA在神经元结构附近局部使用时具有潜在的神经毒性,因此不允许在脊柱手术中局部使用TXA。
(二)床旁定点检测(Point-of-care testing)
目前,床旁定点检测设备是欧洲中心的护理标准,因为它们允许在手术期间和手术后进行充分的引导性血液疗法(adequate guided hemotherapy)。
在美国,则较少使用,主要在中心实验室由实验室技术人员进行操作。它们的使用减少了对血液制品的需求,因此它们增加了患者的安全性并且具有降低成本的较高潜力。
在最近的出版物中,描述了基于实验室资料和床旁定点检测的输血算法引导的目标导向输血治疗。
- 血栓弹性描记图(thrombelastography)和血栓弹力图(thromboelastometry)均能够测量并图像化展示血凝块凝结和降解全过程的黏弹性变化(viscoelasticity)。
- 第一次结果可在5-10分钟内获得,而实验室结果则需30-90分钟内获得,从而延迟了患者的治疗。
最近,Naik等人对接受脊柱手术的患者进行了一项研究。
- 他们比较了接受常规实验室检查(常规组)和ROTEM®(ROtational血栓弹力图)引导凝血管理的患者(ROTEM组)。
- 这两个组均进一步细分为两个亚组,其中一组使用TXA,而另一组则不使用TXA。
- 与仅使用TXA相比,TXA和ROTEM®能够显著降低出血量并减少红细胞的输注(p =0.0005)。
- 根据ROTEM®的分析,冷沉淀(cryoprecipitates)的使用增加,而新鲜冰冻血浆(fresh frozen plasma,FFP)的使用则减少。
低纤维蛋白原血症(hypofibrinogenemia)被确定为持续的凝血病的主要原因(p <0.0002)。
- 因此,在脊柱大手术中,ROTEM®引导的凝血管理允许输血实践的标准化和低纤维蛋白原血症的早期识别和治疗。
- 由于低纤维蛋白原血症是这些干预期间遇到的凝血病的主要原因之一,因此早期对此问题的处理能够减少术中的出血量,减少输血的需求并降低输血相关的成本。
血浆主要成分
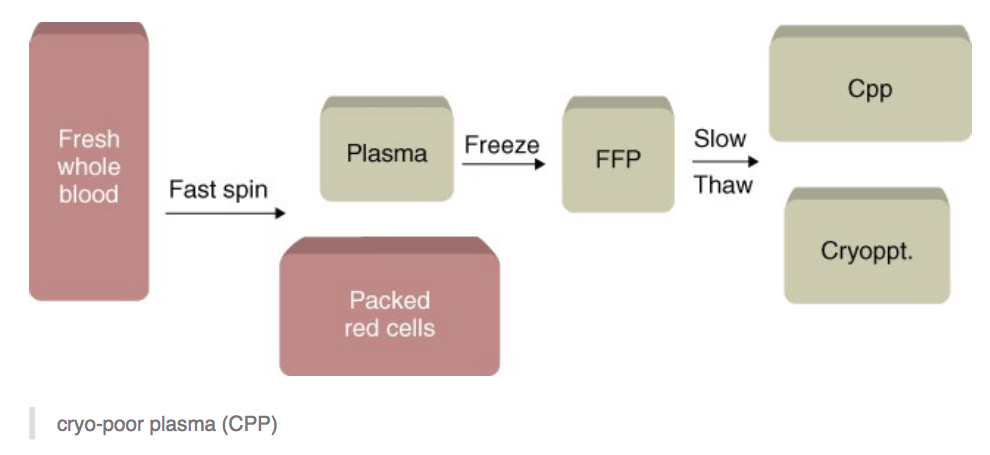
- 新鲜冰冻血浆(fresh frozen plasma, FFP)
- 是全血采集后6小时内分离并立即置于-20~30℃保存的血浆。冰冻状态一直持续到使用之前,有效期为1年。
- 成份:全部的凝血因子+各种血浆蛋白
- (普通)冰冻血浆(frozen Plasma,FP)
FFP在4℃下融解时除去冷沉淀成分冻存的上清血浆制品
成分为FFP-(Ⅴ因子+Ⅷ因子+部分纤维蛋白原,三者含量较FFP低)
新鲜冰冻血浆保存一年后就成为普通冰冻血浆,缺乏不稳定的凝血因子如Ⅴ、Ⅷ等,但其含有稳定的凝血因子
- 冷沉淀(cryoprecipitate,Cryo)
- FFP在4℃下融解时不融的沉淀物,每袋20-30ml
- 成分为:
- 纤维蛋白原(至少150mg)
- Ⅷ因子(80〜120U以上)
- 血管性假血友病因子(vW因子)
- 新鲜冰冻血浆(fresh frozen plasma, FFP)
(三)凝血因子浓缩物(Coagulation factor concentrates)
- FFP的使用会导致不良反应,例如死亡率增加,多器官功能衰竭,感染的风险,肺损伤和免疫调节(immunomodulation)。
- FFP与纤维蛋白原浓缩物(fibrinogen
concentrate)相比,在临床终点上(如出血,输血要求,住院时间和血浆纤维蛋白原浓度),纤维蛋白原浓缩物的有效性显著高于前者。
如前所述,在许多出血性疾病中,低纤维蛋白原血症是第一个达到极低水平的凝血因子。
已经在许多中心提出并实施了对纤维蛋白原浓度的早期测试,特别是对于纤维蛋白原活性(fibrinogen activity)的测试。
在出血的情况下,纤维蛋白原浓度(fibrinogen concentrations)的目标水平应定义为1.5-2.0 g/L,相当于用ROTEM®测量的FIBTEM中7mm的最大血凝块硬度(maximum clot firmness,MCF)
在全血中加入血小板抑制剂(细胞松弛素D,cytochalasin D)进行的试验,以评估纤维蛋白原对形成血凝块的贡献。
- 纤维蛋白原(Fibrinogen)是止血的核心元素,达到这些目标水平尤为重要,特别是在血小板减少(症)(thrombocytopenia)和出血(bleeding)的情况下。。
- 使用纤维蛋白原浓缩物(fibrinogen concentrates)优于FFP输注(FFP transfusion),因为FFP中的纤维蛋白原浓度是高度可变的并且相对较低,平均为2g/L。
- 大量输注FFP对于有效增加纤维蛋白原浓度是必要的,但鉴于FFP中纤维蛋白原的浓度,实现0.2g/L的纤维蛋白原浓度几乎是不可能的。
- 此外,监测因子XⅢ(FXⅢ)的水平至关重要,因为低水平的因子XⅢ(FXⅢ)与出血增加有关。
- 因此,使用FXIII浓缩物时,建议使用60%FXⅢ活性水平。
- 除单因子浓缩物外,凝血酶原复合物浓缩物(prothrombin complex
concentrates,PCC)也是基于因子的算法(factor-based algorithms)的一部分。
- 就所包含的凝血因子而言,个体的PCCs均有所不同,它们的相对组成和血栓形成的潜力方面各有不同。
- 通常,PCCs用于逆转口服抗凝药(oral anticoagulants),这在择期脊柱手术期间不太可能存在。
- 如确实需要,PCC应仅在严格的算法中使用,剂量应小,对重复给药应非常谨慎,以尽量减少血栓形成的风险。
(四)急性贫血(Acute anemia)
- 即使在手术前充分纠正术前贫血,由于血管的解剖结构和大切口,仍然存在脊柱手术期间大量出血的风险。
- 然而,即使没有同种异体输血,患者也可以从严重贫血(血红蛋白低至1.4 g/dl)中恢复而无后遗症。
- 7.0-9.0 g/dl的限制性输血触发(Restrictive transfusion triggers)似乎是足够的。
- 急性贫血耐受似乎是器官特异性的。
- 一项动物试验,分为三个随机组。
- 一组血液没有稀释,剩余两组分别用6%羟乙基淀粉(hydroxyethyl starch) 稀释至血红蛋白值 4.3 g/dl和临界定义的血红蛋白值 2.7 g/dl。
- 实验结果表明:
- 对于心脏,脑和肝脏等器官,血流动力学(Hemodynamics),全身代谢参数(wholebody metabolic parameters)和耗氧量(oxygen consumption)以及组织氧合作用(tissue oxygenation)均未在血红蛋白值为4.3 g/dl时受到损害。
- 肾脏和骨骼肌则显示出在4.3 g/dl水平时受到损伤。
- Pape等人的研究表明,深部神经肌肉阻滞能够增加急性等容性贫血(acute
normovolemic anemia)的耐受性。
- 可能的机制似乎涉及减少骨骼肌氧消耗,从而使重要器官受益。
- 因此,神经肌肉阻滞(deep neuromuscular blockade)可能在急性贫血的治疗中起重要作用,因为可以更好地耐受血红蛋白的临界水平。
- 在脊柱手术中,这种治疗选择并不真正可行,因为脊柱矫正术后的神经系统检查是最重要的,并且大多数患者在术后均已拔管(气管导管)。
(五)去氨加压素(DDAVP)
- 去氨加压素(DDAVP:1-脱氨基-8-D-精氨酸加压素,0.3
mcg/kg)可增强血小板粘附,是治疗下列两类患者的首选:
von Willebrand因子(血管性血友病因子,vWF)数量缺乏(quantitative deficiency) 的(1型)出血患者。
von Willebrand因子质量缺陷的(2型)出血患者。
1-deamino-8-D-arginine vasopressin
微克(microgramme),质量单位,符号μg或者mcg
1,000 微克 = 1毫克,1,000,000 微克 = 1克
- 用阿司匹林和ADP(二磷酸腺苷)受体抑制剂(如氯吡格雷)治疗的患者可以从为评估去氨加压素治疗的个体功效而进行的床旁定点检测中受益。
- 如果使用去氨加压素治疗不充分,则输注血小板是最终的选择。
- 其他抗血小板药物如替格瑞洛(ticagrelor)的作用可能不易被去氨加压素逆转,甚至血小板输注也可能相对无效。
(六)新型口服抗凝药
- 计划进行择期手术的患者越来越多地接受新型口服抗凝药(new oral
anticoagulants)治疗,如:
- 直接凝血酶(direct thrombin)
- 达比加群(Dabigatran)
- Xa因子抑制剂
利伐沙班(rivaroxaban)
阿哌沙班(apixaban)
依度沙班(edoxaban)
通过使用高剂量的PCC(50u/KG bw)可以逆转抗因子Xa效应。
bw即bodyweight
- 直接凝血酶(direct thrombin)
- 在新型口服抗凝药下使用活化的因子Ⅶ来治疗出血是适应证外的并且在很大程度上是无效的。使用这些药物治疗的患者只能延迟手术。
- Glund et al.最近发表了关于达比加群拮抗剂idarucizumab的数据。他们对47名健康男性进行了一项随机,安慰剂对照的双盲试验,结果表明,在没有相关安全问题的情况下,dagibatran的效果可以立即完全逆转。
五、血液保存技术(Blood sparing techniques)
(一)自体预供血(Autologous predonation)
- 自体预供血是一项已开展技术,据报道是安全有效的,减少了腰椎融合和脊柱侧凸手术中对同种异体输血的需求。
- 然而,据Brookfield等人在近700名接受择期脊柱手术患者的回顾性研究中发现:
- 与未预供血的患者相比,预供血的患者(patients with predonation)出现了类似的失血。
- 此外,两组间同种异体输血率无明显差异。
- 这些结果清楚地表明应该放弃这种做法,因为它对大多数患者无效。
- 然而,在罕见血型或广泛抗体的患者中,自体预供血可能仍然是一种选择。
(二)急性等容性血液稀释(Acute normovolemic hemodilution)
- 急性等容性血液稀释在脊柱手术中很常见,并且减少了对脊柱融合以及脊柱侧凸手术中同种异体红细胞输注的需求。
- 另一个好处是,高达30%的急性血液稀释(hemodilution)可能会导致轻度高凝状态(mild hypercoagulable state),从而导致术中出血减少。
- 可用于采集的血液量由每个患者的下列三个因素决定:
- 术前血容量
- 血细胞比容(hematocrit)
- 目标血细胞比容(targeted hematocrit)
(三)术中红细胞回收和再输注(Intraoperative RBC salvage and reinfusion)
- 术中红细胞回收对减少同种异体输血的需求仍存在争议。
- 在几项回顾性研究,meta分析和Cochrane综述中,报道了其在脊柱椎板切除术,融合术或内固定术中的有效性。
- 相比之下,Gause等人的研究表明术中红细胞回收在择期腰椎内固定融合术患者中不仅没有减少RBC输血的需要,而且还与大量失血相关。
- 这种悖论可能是因为外科医生在血液回收存在下的止血(hemostasis)可能变得不那么细致
- 并且再输注的回收血液含有干扰正常凝血的产品(例如肝素/heparin)
- 此外,一项研究表明,术中血液回收的成本超过了接受特发性脊柱侧凸手术治疗给患者带来的益处。
- 当红细胞回收与急性等容行血液稀释进行比较时,当红细胞回收<2单位红细胞时,血液稀释更具成本效益。
- 通常,对于涉及肿瘤,感染或应用一些局部药剂的的外科手术是术中红细胞回收的禁忌。
(四)控制性低血压
- 低动脉血压可减少血液外渗(blood extravasation)和局部伤口血流,从而减少出血。
- 然而,在脊柱手术中出血的两个决定性因素为:
- 硬膜外静脉丛压力(epidural venous plexus pressure)
- 骨内压力(intraosseous pressure)
- 涉及去除骨皮质(bone decortication)
- 上述两者的压力与动脉血压无关,并且控制性低血压技术在脊柱手术中的确切机制和价值仍未知,因为人们对其潜在的并发症更为担忧。
- 术后失明是一个主要问题,估计有0.1%的患者在俯卧位进行脊柱手术。
- 在这些患者中也经常观察到低血压,尽管低血压和失明之间的明确关联仍需进一步明确。
- 因此,对于俯卧位进行手术的患者,应谨慎使用控制性低血压。
- 低收缩压也会影响器官的灌注,包括脊髓。因此,低血压与影响组织氧输送的其他技术(如血液稀释)的结合需要进行适当的评估以避免并发症。
- Monk等人在近20,000名患者的大型队列研究中显示高血压对30天死亡率没有影响。相反,低血压与30天死亡率的增加有关。
- 低血压的定义为:
- 收缩压(systolic pressure)<70 mmHg,且≥ 5 min。
- 平均动脉压(mean arterial pressure)<49 mmHg,且≥ 5 min。
- 舒张压(diastolic pressure)<30 mmHg,且≥ 5 min。
- 平均动脉压较基线水平降低> 50%,且≥ 5 min。
- 这些新发现表明,选择低血压水平需要仔细评估其风险。
(五)温度调节(Temperature regulation)
- 如Michelson等人所示,低温会损害凝血,特别是血小板功能。
- 凝血级联(coagulation cascade)的酶活性/功能受损是第二个问题。
- 轻度低温可以增加手术期间的出血和异体输血要求。
- 在一项随机试验中,Schmied等人比较了行髋关节置换术的患者中,未积极升温(平均核心温度:35℃)与积极升温(平均核心温度:36.6℃)。在较冷的组中发现出血增加30%并且输血也显著增加(p <0.05)。
- meta分析结果表明,核心温度的这种微小差异确实是导致出血和输血需求的主要差异。并且在所有类型的手术中(包括髋关节置换术,心脏手术,腹部大手术和子宫切除术),温度差<1℃与平均出血增加约20%相关,输血的风险平均增加22%。
(六)患者体位
硬膜外静脉通过无瓣静脉系统(valveless venous system)连接到下腔静脉。在俯卧位,腹压增加并引起腔静脉压迫,这增加了硬膜外静脉回路中的压力和术中失血。
Bostman等人的研究显示,与躺在常规枕垫(conventional bolsters)上的患者相比,放置在支撑跪姿支架(a frame in a supported kneeling position)上的患者,其腰椎手术期间术中出血量显著减少(p <0.001)。
Lee et al.研究了位于常规垫上传统俯卧位的患者与位于“Reltone Hall” frame上且腹部无受压患者之间的下腔静脉压差异。在“Reltone Hall” frame上的患者,下腔静脉压明显降低(p <0.05)。
Park发现脊柱手术中腹内压降低与术中出血量之间存在显着相关性。在腹部无受压的患者中,也发现术中总的出血量与手术期间的平均腹内压高度相关。
因此,正确的体位是减少脊柱手术中出血的关键。
(七)手术技术
- 背部的皮肤,特别是颈背部区域的皮肤灌注较好。
- 手术切开后,皮肤边缘渗血很常见。
- 使用低剂量肾上腺素局部皮肤浸润能够减少渗血。
- 椎旁肌的营养血管非常靠近椎体。
- 骨膜下剥离对于最大限度地减少对这些血管的损伤至关重要,从而减少术中出血。
- 因此,术中步骤的正确顺序也有助于减少出血。
- 脊柱融合经常需要对椎体表面骨皮质decortication,从而导致骨出血(bone bleeding)。
- 最后执行这一操作步骤,然后填塞切口,快速不渗血地闭合切口也能够减少出血。
- 手术中仔细止血也可以减少术中和术后出血。
- 应通过热凝固(thermal coagulation)阻止软组织的出血。
- 可以用少量骨蜡阻止骨出血。
- 硬膜外出血通常可以用双极电凝(bipolar diathermy)控制。
- 如果静脉压低,仅通过用盐溶液(saline solution)填充伤口来施加流体静压(hydrostatic pressure)就能够帮助控制硬膜外的静脉出血。
(八)使用局部止血剂
- 不同的局部止血剂可在市场上获得,并分为两大主要类别:
- 被动止血剂:通过接触激活(contact activation)和促进血小板聚集(platelet aggregation)来发挥作用
- 主动止血剂:在凝血级联(clotting cascade)激活后将产生纤维蛋白凝块(fibrin clot)。
- 局部被动止血剂的实例:
- 基于胶原蛋白(Collagen-based)的产品
- 基于纤维素(cellulose-based)的产品
- 基于明胶(gelatin-based)的产品
- 作用机制是提供促进血小板聚集的结构,促进血凝块形成和止血。
- 局部主动止血剂发挥生物学功能并在凝血级联反应结束时直接参与,以在出血部位诱导纤维蛋白凝块的形成。
- 它们包括凝血酶(thrombin)和含有凝血酶和某些被动止血剂的组合产品。
- 所有产品都能迅速起效,并确保大多数患者在10分钟内止血。
- 由于这些药剂直接参与凝血级联的最终生理反应步骤并绕过最初的酶促步骤(enzymatic steps),因此它们的止血作用不易受凝血因子缺乏或血小板功能障碍引起的凝血障碍的影响。
- 虽然局部止血剂能够有效止血和减少出血,但它们有潜在的缺点。
- 被动局部止血的扩大可导致并发症,例如周围组织中骨和坚硬的组织对神经的压迫导致的神经功能损伤。
- 现场残留的产品也可能加剧异物反应(foreign body reaction),慢性炎症或感染,因此一旦出血停止就应该去除。
(九)术后红细胞回收
- 关于脊柱手术后血液回收的研究很少。
- 由于先前的研究将术后血液回收与其他技术相结合,因此缺乏客观的评估。
- Sebastian et al.单独评估术后血液回收,并发现它将同种异体输血减少了30%。
- 未经洗涤的回收血液的再输注不是优选的,因为它含有有害物质,如:
- 细胞碎片(cell debris)
- 骨髓脂肪(marrow fat)
- 纤维蛋白(fibrin)
- 游离血红蛋白(free hemoglobin)
- 但使用40毫米血液过滤器(40-mm blood filters)进行再输注可以解决这个问题。
- 与术中血液回收相反,术后血液回收尚未根据其成本效益进行评估。
六、结论
- 脊柱手术中的血液保护策略是一种多学科方法,结合了不同的技术。
- 除了效果(efficacy),还需要考虑安全性(safety)和成本效益(cost-effectiveness)。
- 需要付出更多努力来为脊柱手术创建标准化的血液保护方案,所有相关方都能接受该方案,并且长期结果的数据证明该方案是有益的。
七、实践要点
- 每个计划进行择期脊柱手术的患者都必须接受贫血筛查。
- 贫血患者应先接受治疗,以达到正常的血红蛋白水平再去做手术。
- 强制性使用氨甲环酸以减少失血。
- 使用全血凝固试验(whole blood coagulation tests),例如血栓弹力测定法(ROTEM)结合算法,并使用凝血因子浓缩物减少了对同种异体输血的需求(红细胞/FFP/血小板)。
- 输血触发应设定为60-80 g/L。